2025年国际神经母细胞瘤研究进展会议(ANR)于5月25日至28日在美国华盛顿召开。会议聚焦神经母细胞瘤(NB)的发病机制、诊疗技术、治疗策略等多方面的进展,旨在为提升NB患者的预后寻求新的思路与方法。GD2作为存在于NB细胞膜表面呈特异性高表达的抗原,成为NB免疫治疗的理想靶点。近年来,随着创新药物的不断发展,靶向GD2的抗体药物为改善NB患者的治疗结局带来了新希望。
此次会议中,共有近40篇关于GD2单抗用于临床治疗NB的研究成果入围展示,本期特别对此次会议上公布的前沿进展进行精要总结,并邀请上海交通大学医学院附属新华医院袁晓军教授进行专家点评,以期为广大读者呈现这一领域的最新动态。
HR-NB早期诱导:
诱导化疗联合GD2单抗免疫治疗新进展
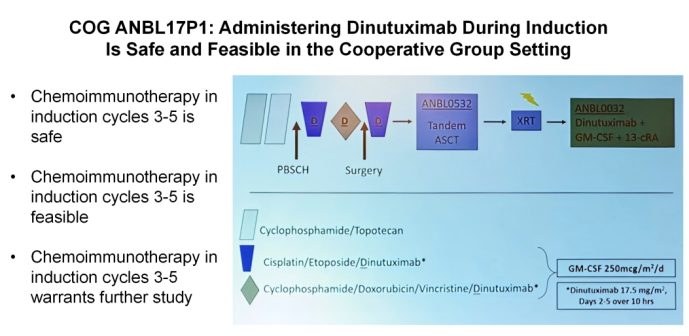
GD2单抗免疫治疗是NB治疗领域的重要研究方向。2021年,达妥昔单抗β在中国获批,适用于初治高危神经母细胞瘤(HR-NB)以及复发/难治性神经母细胞瘤(R/R NB),推动NB治疗模式向靶向精准化转变。COG ANBL17P1研究中[1],于诱导阶段的第3-5个治疗周期接受GD2单抗达妥昔单抗与化疗联合的化学免疫疗法(CIT),并在维持治疗阶段继续使用达妥昔单抗(治疗方案详见图1);在结束治疗后检测到的人抗嵌合抗体反应(HACA)水平(13.3%强阳性HACA和6.7%中和性HACA),与ANBL0032研究中仅在维持治疗阶段接受达妥昔单抗治疗的HACA发生率(8.8%强阳性HACA和6.6%中和性HACA)相近,表明早期使用达妥昔单抗并未增加后期维持治疗HACA发生率,支持其在诱导阶段的应用。
图1. COG ANBL17P1研究:诱导期化疗联合达妥昔单抗治疗方案
(来自ANR 2025.Novel Therapies and Emerging Horizons in High-risk Neuroblastoma Management.Symposium Slides)
本次2025 ANR会议上,还重点披露了两项围绕达妥昔单抗β用于HR-NB患者CIT诱导治疗的临床研究。一项是来自俄罗斯的前瞻性临床研究[2],公布了13例新诊断的HR-NB患者行CIT诱导治疗的安全性数据。研究采用改良GPOH NB2004方案,从第3个诱导周期开始,共接受4个周期的N5/N6化疗联合达妥昔单抗β治疗,达妥昔单抗β剂量为10 mg/m /天,连续输注5天。共完成52个CIT治疗周期,结果显示研究期间未发生严重的意外毒性事件或死亡事件,安全性良好;且61.5%的患者达到至少部分缓解(PR),即1例为完全缓解(CR)、4例非常好的部分缓解(VGPR)、3例PR。
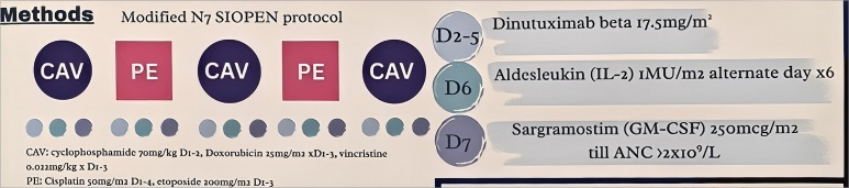
另一项为来自中国香港的研究[3],评估了HR-NB患者接受达妥昔单抗β联合诱导化疗在诱导治疗结束时的缓解率。该研究采用以改良N7 SIOPEN方案为诱导化疗,联合达妥昔单抗β、沙格司亭(GM-CSF)、阿地白介素(IL-2)(治疗方案详见图2)。结果显示,总体缓解率达85.7%(6/7),包括6例(85.7%)原发肿瘤达到至少PR,5例(71.4%)转移灶实现完全缓解(mCR)。这两项研究显示出达妥昔单抗β联合化疗的CIT在HR-NB诱导治疗阶段的良好安全性及肿瘤缓解率,支持这一治疗策略在更大规模的Ⅲ期研究中进一步验证,以期为提高HR-NB治愈潜能提出更优的治疗方案。
图2. 改良N7 SIOPEN方案:诱导期化疗联合达妥昔单抗β治疗方案
(来自Evelyn Lu,et al.Presented in Poster.ANR 2025.)
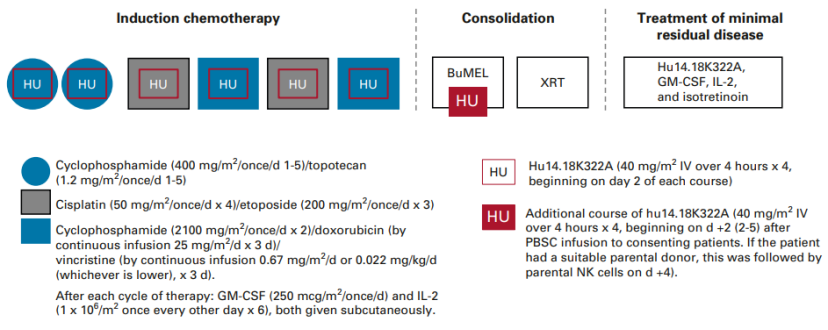
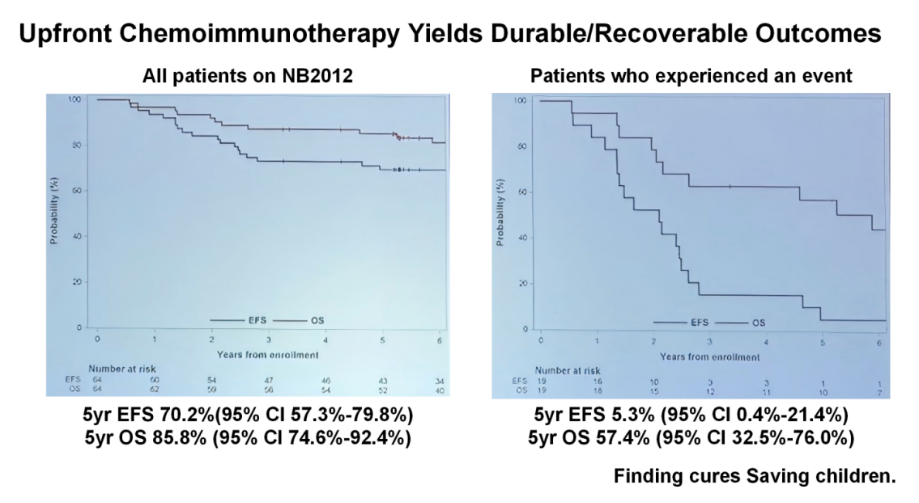
此外,还有一项来自St.Jude儿童研究医院研究报道,更新了在诱导化疗中加入GD2单抗hu14.18K322A 的Ⅱ期研究(NCT01857934)的5年长期随访结果[4]。共纳入64例患者,基于NB2012方案的诱导化疗联合hu14.18K322A治疗(具体方案见图3),能够显著提升HR-NB患儿的长期生存,5年无事件生存(EFS)率达70.2%,5年总生存(OS)率达85.8%(请见图4),无事件中位持续时间达7.9年。该研究还揭示了TERT基因重排、11号染色体长臂杂合性缺失(11q LOH)及男性为独立危险因素,这将为NB的精准分层治疗提供了新的依据。
图3. 研究治疗方案(Fuman W, et al. JCO,2021)
图4. 总体患者及复发/进展性患者的生存分析
(来自Megan Lilley, oral presentation, ANR 2025.Slides)
R/R NB: GD2单抗
免疫联合化疗的研究进展
复发一直是NB治疗中最棘手的临床问题,即使接受前期多模式治疗后,约60%的患者仍会复发,其5年总生存率仅20%左右[5]。因此,降低NB复发风险是当前临床的迫切需求。随着对GD2单抗的研究不断深入,其联合化疗治疗R/R NB带来的积极抗肿瘤活性获得广泛关注。本次ANR 2025会议上,也有多项研究聚焦基于GD2单抗的免疫联合疗法在R/R NB的应用探索,以期获得更好的临床结局。
美国的一项回顾性研究[6]分析了54例接受拓扑替康/环磷酰胺/达妥昔单抗(T/C/DIN)治疗的R/R NB患者,包括49例复发患者以及5例难治患者,其中89%曾接受伊立替康/替莫唑胺/达妥昔单抗(T/I/DIN)治疗方案。结果显示,42.6%的患者经T/C/DIN治疗后至少达微小缓解(MR);既往对T/I/DIN有反应者接受T/C/DIN治疗方案的客观缓解率(ORR)更高,达54%,提示该方案可作为挽救治疗的可行选择。
另有两项研究分别探索了T/I/DIN方案治疗R/R NB患者的长期随访结果及创新联合治疗策略。ANBL1221研究更新了T/I/DIN方案治疗首次复发/进展或难治性患者的长期随访结果[7], 5年无疾病进展(PFS)率和5年OS率分别为22.6%±6.6%和54.7%±7.7%。研究还发现,长期及短期生存患者在临床和肿瘤生物学特征上相似,未来仍需进一步探索新型标志物,以识别可能在该方案治疗下长期生存的患者。一项T/I/DIN方案联合万能供体NK细胞治疗R/R NB的Ⅰ期临床研究[8]显示,4例患者接受最多6个周期,观察到最佳治疗反应为1例CR、2例PR和1例SD,安全性方面仅1例患者接受2次NK细胞输注后出现1级发热,未观察到其他归因于NK细胞的不良事件。
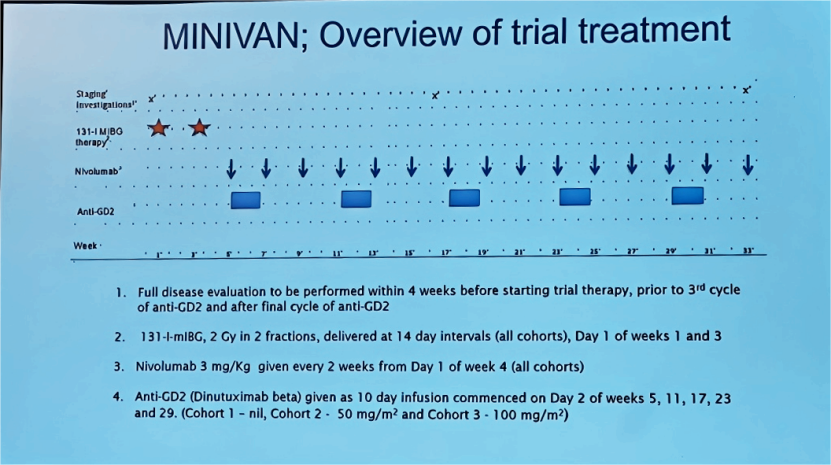
一项临床前研究[9]则证实,达妥昔单抗β联合抗TIGIT和抗PD-L1双抗体可显著增强抗体依赖的细胞介导的细胞毒性作用(ADCC),提升抗肿瘤效果,为HR-NB提供了新型组合策略。MINIVAN研究(NCT02914405) [10]评估了R/R NB患者采用131I-mIBG治疗后接受达妥昔单抗β联合纳武利尤单抗(3mg/kg,每2周一次)的有效性和安全性(治疗方案详见图5),根据达妥昔单抗β治疗情况共分为三个队列,分别为队列1无达妥昔单抗β治疗、队列2达妥昔单抗β 50 mg/m2、队列3达妥昔单抗β 100 mg/m2,均是连续输注10天。共43例患者入组,其中队列1为7例,队列2为6例,队列3为30例。研究结果显示,队列1和2的总体肿瘤缓解率(包括PR和CR)为16.6%,队列3则提升至42.9%;毒性反应方面,队列1和2均可耐受,队列3中有4例因毒性反应停止治疗,总体安全性较好。该初步数据支持这一联合方案的临床可行性。
图5. MINIVAN研究治疗方案
(来自Prof. JC Gray. Oral Presentation.ANR 2025.Slides)
此外,还报道了SACHA-France真实世界研究[11],分析了基于达妥昔单抗β的CIT作为二线方案用于高剂量化疗(HDC)前出现疾病进展(PD)的ALK野生型HR-NB患者的疗效及安全性。结果显示,38%(5/13)的患者观察到客观缓解,4例早期进展患者中有3例达到PR,其中包括2例N-MYC扩增患者。3例接受HDC的患者均未出现PD超1年。提示CIT可使早期PD的HR-NB患者获益,包括在诱导化疗期间或结束时出现进展及伴有N-MYC基因扩增的患者。
综上,当前的研究正在通过优化化疗药物组合、联合免疫检查点抑制剂抗PD-1,或者抗TIGIT、131I-MIBG治疗等方案,不断探索提高R/R NB肿瘤缓解和生存获益的新方法。
GD2单抗达妥昔单抗β
治疗方案优化的研究新进展
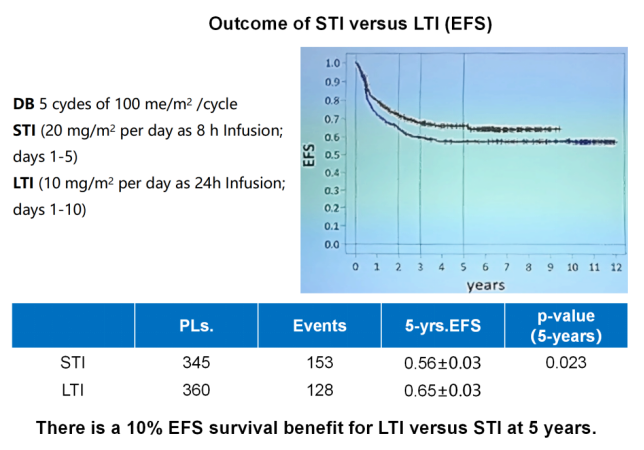
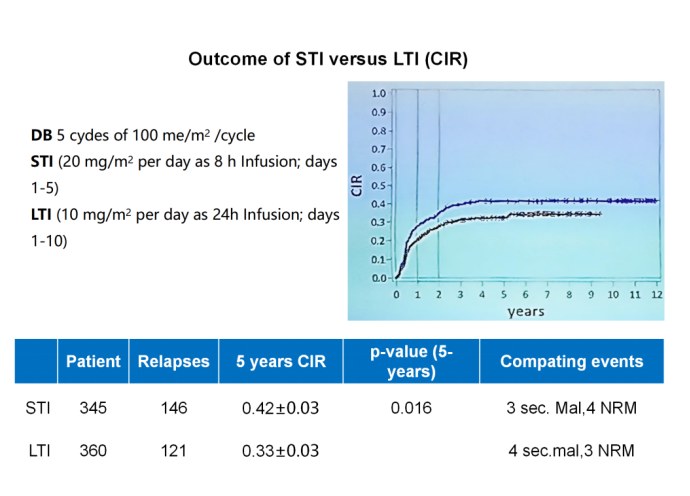
本次ANR 2025会议上,关于达妥昔单抗β在输注时长、机制优势方面的探索,也有数项研究进行了报道。HR-NBL1/SIOPEN研究比较了达妥昔单抗β短期输注(STI)与长期输注(LTI)方案的疗效和安全性[12]。结果显示,LTI组的5年EFS率显著高于STI组(65%±3% vs. 56%±3%,P=0.023),LTI组的累积复发率(CIR)显著低于STI组(33%±3% vs. 42%±3%,P=0.016)(请见图6);LTI相较于STI可显著减少包括疼痛、中枢神经毒性、低血压、超敏反应等不良反应,提升治疗安全性。该研究结果表明,达妥昔单抗β LTI 10 mg/m /天连续输注10天,可作为HR-NB及R/R NB患者的一种耐受性良好且具有临床优势的治疗方式。
图6. 达妥昔单抗β采用LTI与STI方案的治疗结局比较
(来自Prof. HN Lode.ANR 2025.Oral Presentation.Slides)
还有研究发现[13],Fcγ受体多态性(FCGR)和自然杀伤细胞(NK细胞)数量可作为ADCC的替代指标,对于识别达妥昔单抗β治疗的患者预后具有应用价值。此外,一项机制研究比较了两种GD2单抗的抗肿瘤效应[14],中等亲和力的达妥昔单抗β由于受靶标介导的药物处置(TMDD)效应影响较弱,其ADCC效力表现要优于高亲和力抗体Naxitamab。
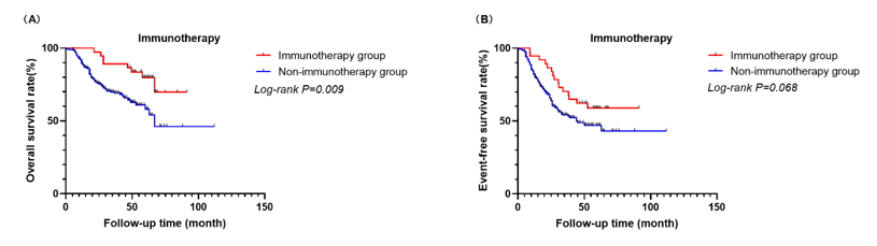
此次ANR 2025会议上,也有数项国内学者的高质量研究成果亮相。来自上海新华医院牵头的一项多中心临床研究报道了达妥昔单抗β“先行先试”用药的37例HR-NB患者的远期随访结果[15],其中包括了26例初治高危和11例复发/难治患者,中位随访时间达57.8个月。通过与未接受免疫治疗的277例高危患者进行比较,接受达妥昔单抗β免疫治疗的HR及R/R NB患儿5年OS率显著优于非免疫治疗组(78.7%±7.4% vs. 58.1%±4.9%,P=0.009),5年EFS率也存在免疫治疗组高于非免疫治疗组的趋势(77.0%±7.2% vs.55.6%±6.2%,P=0.068)(请见图7)。HR-NB组ORR为76.9%,较R/R NB组ORR为36.4%明显更高(P=0.047)。可以看出,达妥昔单抗β在中国NB患儿中展现出令人鼓舞的疗效,提示达妥昔单抗β是一种具有前景的治疗策略,可改善HR及R/R NB患儿的预后。
图7. 达妥昔单抗β免疫治疗与非免疫治疗组的OS(A)及EFS(B)比较
(来自Jiaxi Du, et al. Presented in Poster. ANR 2025.)
来自山东省肿瘤医院报道了51例新诊断HR-NB患者接受达妥昔单抗β一线维持治疗的疗效与安全性[16],总体2年EFS率达80.1%,2年OS率达97.6%。该研究提出了对于PR及VGPR(除外仅骨髓残留)使用达妥昔单抗β联合长春新碱/伊立替康/替莫唑胺(VIT)化疗的治疗策略,ORR达60.6%,CRR达54.5%,且安全性好,这表明了联合VIT化疗对于维持治疗前未达CR的患者是一种可能的治疗选择。此外,山东省肿瘤医院另外一项研究分析了54例R/R NB患者接受达妥昔单抗β免疫治疗的临床疗效[17],所有患者接受1~12周期(中位周期数:6)达妥昔单抗β联合或不联合化疗,研究结果显示总体ORR达55%,1年PFS率为74.3%,1年OS率为95.7%。
来自北京京都儿童医院的研究也评估了达妥昔单抗β治疗中国R/R NB患儿的疗效与安全性[18]。研究中12例R/R NB患儿共完成了57个周期的达妥昔单抗β治疗,8例患者获得缓解,短期疗效及耐受性较好,有待于进一步长期随访。
专家点评
此次2025年ANR会议上公布了为数众多的关于GD2单抗治疗神经母细胞瘤的亮点研究。这些研究不仅有望为临床治疗提供新的方案与选择,同时也展现了国内外学者在这一领域新的思考与突破。
在治疗策略方面,GD2单抗与化疗联合的CIT展现出显著疗效,有效提升了HR-NB患者的诱导阶段肿瘤缓解。同时,针对R/R NB患者,多种创新性的联合疗法也在改善抗肿瘤疗效及患者生存获益方面取得了一定的进展。此外,研究者们通过对达妥昔单抗β输注模式的比较,以及基于生物标志物的疗效预测探索,为进一步提升GD2单抗的疗效及优化神经母细胞瘤的精准治疗奠定了基础。
从当前的研究进展可以看出,GD2单抗用于HR-NB及R/R NB的治疗关口前移成为重要趋势,且NB患者的个体化治疗需求日益凸显,生物标志物或能帮助进一步识别优势人群,并为治疗获益受限的患者提供替代方案的选择方向。此外,加强真实世界长期疗效的随访,对于巩固新疗法的临床价值同样至关重要。
在各方共同努力下,我国成功获得2027年ANR上海会议的主办权,这标志着我国在神经母细胞瘤领域国际影响力的进一步提升,也是推动该领域在国内发展的重要机遇。中国学者可以聚焦具有本土特色的治疗方案探索,建立患者长期随访体系,进一步助力GD2单抗联合疗法突破HR-NB及R/R NB患者的治疗瓶颈。期待在未来,中国学者能够不断为神经母细胞瘤诊疗体系的完善贡献更多的创新观点与研究成果。
投资查询工具,十大杠杆炒股平台排名,十大配资平台查询提示:文章来自网络,不代表本站观点。